|
El ovario es una máquina del tiempo. Viaja al
futuro y llega a la vejez antes que el resto del cuerpo. Al
nacer, cada ovario contiene alrededor de un millón de folículos,
pequeños sacos llenos de líquido que contienen óvulos inmaduros.
Pero la disminución de estos folículos es inmediata e incesante.
En la pubertad, solo quedan unos 300 mil folículos. A los
40 años, la gran mayoría ya han desaparecido. Y a los 51,
la edad promedio de la menopausia en Estados Unidos y Latinoamérica,
prácticamente no queda ninguno. Los humanos somos una rareza
en este sentido. La mayoría de los mamíferos siguen siendo
fértiles hasta el final de sus vidas; las únicas especies
conocidas que experimentan la menopausia de forma natural
son los humanos y algunas ballenas. En los humanos, la pérdida
de hormonas durante la menopausia desencadena una serie de
efectos negativos para la salud: los huesos se vuelven quebradizos,
el metabolismo se hace más lento y aumenta el riesgo de enfermedades
cardiovasculares, diabetes, derrames cerebrales y demencia.
Paradójicamente, las mujeres viven más que los hombres en
promedio, pero pasan más años con una mala salud.
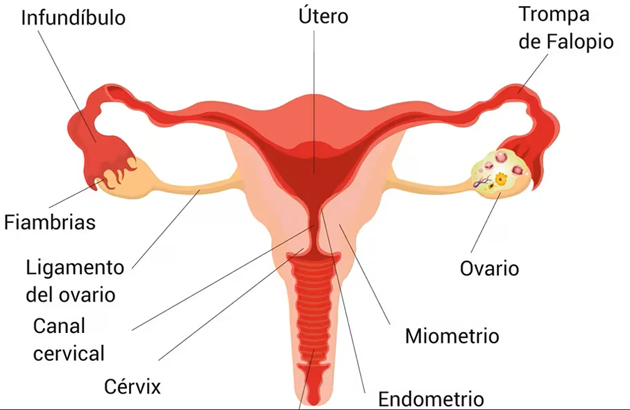
Los ovarios son órganos productores de células
sexuales y hormonas. De su buen funcionamiento depende la
fisiología femenina y la vida reproductiva de la mujer.
Jennifer Garrison tiene la corazonada de que
los ovarios son los culpables. "Ese coctel, esa orquesta de
sustancias químicas que fabrican los ovarios, es verdaderamente
importante para la salud en general", destaca Garrison, profesora
adjunta del Instituto Buck de Investigación sobre el Envejecimiento
de Novato (California). "Cuando desaparece en la menopausia,
tiene un efecto dramático". Por otra parte, tener ovarios
en funcionamiento durante más tiempo parece conllevar beneficios
para la longevidad. Un estudio con 16 mil mujeres descubrió
que una menopausia más tardía aumentaba las probabilidades
de vivir hasta los 90 años. A pesar de que la mitad de la
población mundial experimenta el envejecimiento ovárico, incluidas
las mujeres cisgénero y las personas trans y no binarias,
el persistente sesgo de género en la ciencia significa que
sigue siendo un campo poco estudiado. Pero eso está empezando
a cambiar. Garrison es miembro del Centro de Longevidad Reproductiva
e Igualdad del Instituto Buck, una instalación pionera en
su tipo creada en 2018 con una donación de seis millones de
dólares de la abogada y filántropa Nicole Shanahan. En 2019,
ayudó a lanzar un esfuerzo relacionado, el Consorcio Global
para la Longevidad Reproductiva y la Igualdad, para financiar
a investigadores externos. Inicialmente, 22 investigadores
recibieron subsidios iniciales por un total de 7.4 millones
de dólares. Su objetivo es comprender por qué los ovarios
parecen estar estrechamente relacionados con la salud y la
longevidad.


Desvelar estos misterios podría significar prolongar
los años reproductivos de una persona, y posiblemente su vida,
retrasando la menopausia. En 2018, el estudio de la longevidad
reproductiva era tan incipiente que a Garrison le costó encontrar
profesores a quienes entrevistar, por no hablar de contratar,
para dotar de personal al centro. Pocas personas se dedicaban
activamente a investigarla, en parte porque los únicos mamíferos
que la experimentan son las ballenas, que no pueden analizarse
precisamente en un laboratorio. También es difícil estudiar
el envejecimiento ovárico en especies tan longevas, las orcas,
por ejemplo, pueden vivir hasta 90 años en libertad. En cambio,
los investigadores han intentado muchas veces descifrar la
relación entre la menopausia y el envejecimiento por aproximación:
observando los efectos de la quimioterapia sobre la fertilidad,
estudiando un tratamiento común de la menopausia que imita
las hormonas femeninas o experimentando con ratones, que son
sustitutos imperfectos de los humanos.
Cinco años después, los esfuerzos del Instituto
Buck empiezan a dar resultados. Quizá los investigadores aún
no hayan descubierto cómo retrasar el envejecimiento reproductivo,
pero han despertado el interés por un órgano ignorado durante
mucho tiempo y han abierto una nueva vía de investigación
que podría tener implicaciones para el envejecimiento de todos,
no solo de las personas con ovarios. "Si podemos entender
lo que ocurre en el ovario", indica Garrison, eso probablemente
nos dirá algo sobre el envejecimiento en el resto del cuerpo,
y también podría darnos una idea de cómo intervenir. Para
determinar a qué velocidad envejecen los ovarios, hay que
analizar muchas células. En la Universidad de Columbia (Nueva
York), la genetista Yousin Suh y sus colegas han recopilado
y analizado células extraídas de los ovarios de mujeres en
sus veinte, cuarenta y cincuenta años que aún no han llegado
a la menopausia. Lo que descubrieron les sorprendió. Las células
de los ovarios de mujeres de mediana edad con frecuencia se
parecían a las células de otros tejidos de personas de setenta
años o más. En un tipo de célula tras otro, el equipo de Suh
halló señales inconfundibles de envejecimiento. Observaron
ADN dañado y mitocondrias disfuncionales, las centrales energéticas
de las células. La comunicación entre las células se interrumpió.
Dejaron de dividirse. Un regulador clave del crecimiento y
el metabolismo celular, llamado mTOR, también estaba hiperactivo.
El exceso de mTOR se asocia al cáncer y al envejecimiento,
y los medicamentos que lo inhiben se utilizan para frenar
el crecimiento tumoral. Para Suh, se trataba de una prueba
"clarísima" de que el ovario envejece más rápido que el resto
del cuerpo a nivel molecular y celular. Suh y su equipo publicaron
sus hallazgos en internet el año pasado, y el artículo está
siendo revisado por expertos. El descubrimiento de mTOR fue
particularmente intrigante. Ya se ha demostrado que el bloqueo
de esta proteína aumenta la esperanza de vida en moscas, gusanos
y ratones. Ahora Suh se pregunta si los mismos beneficios
podrían aplicarse a los ovarios humanos.
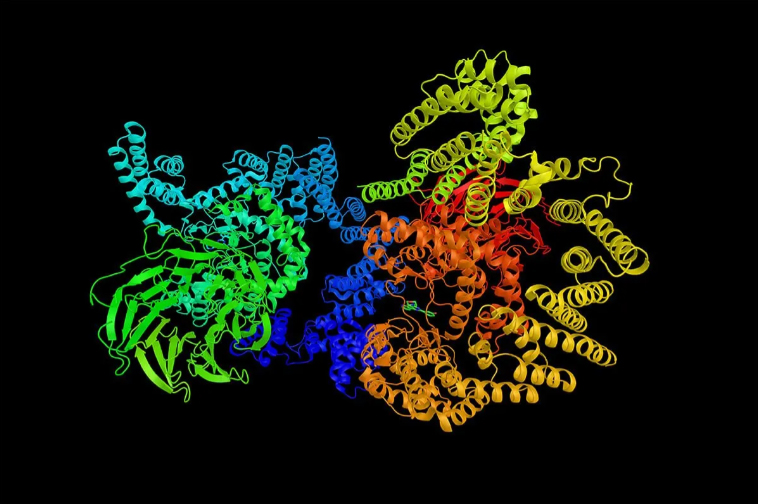
mTOR es la proteína que ayuda a controlar varias
funciones celulares, incluso la multiplicación y la supervivencia
de las células; se une con la rapamicina y otros medicamentos.
mTOR es más activo en algunos tipos de células cancerosas
que en las células normales.
En la Universidad Northwestern de Illinois,
Kara Goldman, profesora asociada de obstetricia y ginecología,
también estudió la relación entre mTOR y el envejecimiento
ovárico. Le interesaba saber si los inhibidores de mTOR podrían
proteger los ovarios contra la pérdida de fertilidad causada
por la quimioterapia. En un estudio de 2017, administró los
medicamentos a ratones hembra por lo demás sanos que también
fueron tratados con quimioterapia. Se esperaba que los animales
tratados con mTOR estuvieran mejor protegidos contra el daño
ovárico que aquellos que solo recibieron quimioterapia. Y
funcionó. Ambos grupos perdieron folículos a causa de la quimioterapia,
pero los ratones que recibieron inhibidores de mTOR conservaron
más folículos. Esos especímenes llegaron a tener más del doble
de crías. En otras palabras, los fármacos parecían preservar
los ovarios, señala Goldman, directora de la junta asesora
clínica del consorcio de Buck. Goldman llevó la investigación
un paso más allá. Quería comprobar si estos medicamentos podían
potenciar la fertilidad en ratones sanos. Administró dosis
orales diarias de inhibidores de mTOR a ratones hembra durante
cuatro semanas, a partir de la edad adulta. Cuando estos animales
se aparearon, procrearon el doble de crías en un periodo de
siete meses que un grupo de control que no recibió los fármacos,
lo que sugiere que se reproducían mejor que los ratones no
tratados.

El cáncer y el tratamiento del cáncer a veces
pueden hacer que tener un hijo resulte más difícil, o pueden
generar dudas sobre si tener un hijo es lo correcto. Las personas
con determinados tipos de cáncer o quienes reciben tratamiento
contra el cáncer pueden tener estas dudas o presentar problemas
de infertilidad.

Ella y su equipo también querían asegurarse
de que los medicamentos no tuvieran efectos secundarios negativos:
un fármaco que se utilizara en personas normalmente sanas
para prolongar la vida útil de sus ovarios tendría que ser
extremadamente seguro, afirma. Su equipo controló la salud
y la fertilidad de los ratones tratados, así como de su descendencia
de primera y segunda generación, y hasta ahora no ha detectado
efectos nocivos. Los investigadores presentaron resultados
preliminares en 2021 y aún están analizando la información.
Pero, ¿sucederá lo mismo con los humanos? Para averiguarlo,
Suh y su colaborador Zev Williams iniciaron un estudio para
comprobar si el medicamento rapamicina, un inhibidor de mTOR,
puede retrasar el envejecimiento de los ovarios. Planean reclutar
a 50 mujeres de entre 30 y 40 años que no planeen tener más
hijos. Durante un año, la mitad tomará diariamente pastillas
de rapamicina y la otra un placebo. Después, los investigadores
comprobarán el número de óvulos sanos que les quedan. Su esperanza
es que el grupo que toma rapamicina tenga más óvulos. Eso
significaría que sus ovarios envejecen a menor velocidad de
lo normal. "Lo que intentamos es retardar el ritmo al que
se pierden los óvulos", declara Williams, director del Centro
de Fertilidad de la Universidad de Columbia. El hecho de que
los ovarios envejezcan mucho más rápido que otros tejidos
corporales también los convierte en un valioso instrumento
para probar medicamentos antienvejecimiento. Este tipo de
estudios podrían aportar información en un plazo de tiempo
mucho más corto que los realizados en otros tejidos del organismo,
lo que podría influir en el envejecimiento tanto de las mujeres
como de los hombres. En definitiva, Goldman ve un futuro en
el que las mujeres tomarían estos fármacos a una edad aún
más temprana. "La idea es no solo proteger la fertilidad,
sino prolongar la salud de los ovarios", resalta.

Miriam Menkin, la científica que cambió la fertilidad
humana para siempre (y qué tuvo que ver una siesta en ello).

Nadie sabe a ciencia cierta si es posible mantener
los ovarios en funcionamiento durante más tiempo, ni si eso
conducirá a una vida más larga y saludable. Los ratones, por
lo menos, parecen beneficiarse cuando sus ovarios se mantienen
sanos durante más tiempo. Cuando investigadores de la Universidad
Estatal de Utah trasplantaron los ovarios de ratones jóvenes
a ratones de más edad, las receptoras vivieron un 40% más
que sus compañeras y también tenían corazones de aspecto más
sano. Pero confiar en los ratones como sustitutos de las personas
tiene un problema: como la mayoría de los animales, los ratones
no pasan por la menopausia. Bérénice Benayoun, profesora adjunta
de gerontología en la Universidad del Sur de California, está
tratando de manipular genéticamente la menopausia en ratones
para que los científicos puedan estudiar los mecanismos biológicos
que la provocan y descubrir cómo contrarrestarla. "La menopausia
es básicamente el acontecimiento más importante en la vida
de una mujer desde el punto de vista de la salud", subraya
Benayoun, financiada por el Instituto Buck.
Otros investigadores han intentado inducir un
estado similar a la menopausia en ratones de dos o tres meses
extirpándoles los ovarios o inyectándoles una sustancia química
para impedir que funcionen. Pero Benayoun considera que es
como intentar que los adultos jóvenes se vuelvan menopáusicos
de repente. Los animales no muestran una pérdida gradual de
la función ovárica a lo largo del tiempo, como los humanos.
Benayoun y su equipo eliminaron en ratones un gen que, en
humanos, provoca una menopausia precoz. En los ratones, la
pérdida de hormonas es más gradual. La investigación aún no
se ha publicado, pero Benayoun piensa que puede ofrecer una
aproximación más cercana a lo que ocurre en los humanos: "podemos
obtener estados hormonales muy similares a los descritos en
las mujeres humanas", puntualiza. Un tratamiento habitual
de la menopausia puede ofrecer algunas claves. La terapia
de reemplazo hormonal (THS, por sus siglas en inglés), suministra
al organismo el estrógeno y la progesterona que dejan de producirse
durante la menopausia. Aunque en general se considera segura
para la mayoría de las mujeres, puede aumentar ligeramente
el riesgo de coágulos sanguíneos e infarto, así como algunos
tipos de cáncer de mama y ovario. Pero los ovarios producen
muchas más sustancias químicas y moléculas de señalización
que estas dos hormonas.
La menopausia es la época de la vida de una
mujer en la cual deja de tener menstruaciones. Suele ocurrir
naturalmente, con mayor frecuencia después de los 45 años.
La menopausia se produce porque los ovarios de la mujer dejan
de producir las hormonas estrógeno y progesterona.
Para Garrison, el problema de la THS es que
no reproduce totalmente el trabajo de los ovarios. Aunque
considera que la THS es "el mejor tratamiento rápido que tenemos",
la considera "sumamente imperfecta" porque no imita todas
las sustancias químicas que produce el ovario. "Ni siquiera
sabemos cuáles son, y mucho menos cómo sustituirlas", aclara.
Quizá el mayor misterio de la menopausia sea por qué los seres
humanos la experimentan. La hipótesis de la abuela, un concepto
propuesto en la década de 1960, sugiere un beneficio evolutivo.
Sostiene que la menopausia permite a las mujeres mayores cuidar
de sus nietos, aumentando así las posibilidades de supervivencia
de sus parientes y garantizando la continuidad de su propio
linaje. Mediante el estudio de las orcas, que también experimentan
la menopausia, los investigadores han descubierto que la presencia
de una abuela viva aumenta las posibilidades de supervivencia
de una cría. Si la teoría es correcta, este mecanismo evolutivo
podría seguir siendo útil para las familias humanas, pero
no tanto para el individuo. Los seres humanos viven más años
y forman familias más tarde que nunca. Las personas nacidas
hoy pueden vivir tanto tiempo después de la menopausia como
antes. ¿Por qué esos años postmenopáusicos no iban a empezar
más tarde y ser más sanos? "La realidad es que la edad de
la menopausia está reñida con la vida moderna", observa Goldman.
Tal vez la menopausia sea inevitable, pero Garrison
cree que es posible por lo menos retrasarla para ayudar a
las personas a mantenerse más sanas en la vejez. Con su iniciativa
en el Instituto Buck, intenta llenar las enormes lagunas creadas
por el sexismo en la ciencia y la recurrente falta de financiamiento
de la investigación sobre la salud de la mujer. Tradicionalmente,
los investigadores han recurrido demasiado a animales de laboratorio
machos y han excluido con frecuencia a las mujeres de los
estudios médicos y toxicológicos, al generalizar a dicho género
a partir de datos obtenidos de hombres. Hoy en día, los ensayos
clínicos están más equilibrados en cuanto al género y, en
2014, los Institutos Nacionales de Salud de Estados Unidos
anunciaron una iniciativa para equilibrar el sexo en los estudios
con células y animales. Aun así, queda mucho por hacer. "No
tenemos muchos conocimientos básicos porque esta área ha sido
ignorada por la comunidad de investigación biomédica durante
mucho tiempo", comenta Garrison. Ahora, el campo del envejecimiento
reproductivo femenino está recibiendo, por fin, la atención
que merece. "Son problemas que tienen solución", añade. Solo
tenemos que hacer el trabajo.
--------------------------------------------------------------------------------------------------------------








--------------------------------------------------------------------------------------------------------------
|
